Transplantace a podpůrné systémy
Úvod do transplantace srdce
Transplantace srdce, neboli přesněji ortotopická allotransplantace srdce, je dnes již zavedenou metodou terapie terminálního srdečního selhání. První snahy o transplantaci srdce se objevují již na začátku 20. století, kdy Alexis Carrel provedl první heterotopickou transplantaci u psa. Koncept ortotopické transplantace u člověka a její operační techniku navrhnul v roce 1960 Norman Shumway. Touto metodou byla u člověka provedena první xenotransplantace šimpanzího srdce v roce 1964 Jamesem Hardym. Technicky byla úspěšná, ale dárcovské srdce selhalo při objemovém přetížení. První allotransplantaci (tj. srdce od lidského dárce) provedl Christiaan Barnard v Jihoafrické republice v roce 1967. Tyto pionýrské operace však byly zatíženy neuspokojivými dlouhodobými výsledky. Od transplantací srdce bylo proto až na výjimky upuštěno, a to až do zavedení imunosupresiva (cyklosporinu) do medicínské praxe v 80-tých letech 20. století, kdy začal celosvětově nový rozvoj transplantací srdce s již dobrými dlouhodobými výsledky.



V současnosti je transplantace srdce široce akceptovanou léčebnou modalitou s uspokojivými dlouhodobými výsledky, jako stran mortality, tak i stran morbidity a kvality života pacientů. Každoročně se na světě uskuteční víc než 5 000 transplantací, sumárně od roku 1982 jich bylo vykonáno téměř 140 000. Specifickým problémem transplantologie je nedostatek dárců při pořád delší čekací listině. Osobitou kategorii tvoří náročný dlouhodobý management pacienta po transplantaci, problematika rejekce štěpu a pozdní komplikace imunosupresivní terapie.
PŘÍJEMCE
Výběr vhodného příjemce pro srdeční transplantát je kruciální součástí celého procesu transplantace. Indikací k provedení transplantace je terminální („end-stage“) srdeční selhání se závažnými symptomy a špatnou prognózou (pravděpodobnost přežití 1 roku <50%). Jsou vyčerpány všechny ostatní terapeutické možnosti, počínaje maximální medikamentózní terapií, přes eventuální revaskularizační procedury, až k zavedení biventrikulárních kardiostimulátorů nebo ICD. Přesná kritéria závažnosti srdečního selhání jsou různé pro transplantační programy různých center, zahrnují však většinou:
- nízká ejekční frakce levé komory (LVEF <20%)
- snížená vrcholová spotřeba kyslíku při zátěži (pVO2 max<15 ml/kg/min)
- vysoký tlak krve v zaklinění v plicním řečišti (PCWP >25 mmHg)
- zvýšená plasmatická hladina noradrenalínu (>600 pg/ml)
- zvýšená hladina N-terminálního proBNP (>5000 pg/ml)
- srdeční arytmie
První dvě charakteristiky jsou považovány za nejspolehlivější prediktory dlouhodobého přežití. Samotnou příčinou srdečního selhání je nejčastěji dilatační kardiomyopatie, hned za ní je na druhém místě srdeční selhání při ischemické chorobě srdeční (spolu tvoří 90% indikací). Ke vzácnějším indikacím patří chlopenní postižení srdce (2-3%), vrozené srdeční vady v dospělosti (2%), re-transplantace (2-3%) a jiné.
Každý potencionální příjemce musí podstoupit podrobné vyšetření s cílem co nejdokonalejšího zhodnocení zdravotního stavu a minimalizace ev. pooperačních komplikací. Vyšetření zahrnuje standardní klidové EKG, EKG Holter monitoring, echokardiografii, zátěžové vyšetření kardiopulmonální kapacity (s cílem zhodnocení vrchlové sprotřeby kyslíku), pravostrannou srdeční katetrizaci (zhodnocení plicní hypertenze), koronarografii (v případě ischemické choroby srdce), neuropsychiatrické vyšetření a vyjádření sociálního pracovníka (ke zhodnocení schopnosti pacienta a jeho blízkých spolupracovat při náročném potransplantačním managementu), biochemické a hematologické vyšetření krve, imunologické vyšetření séra - PRA (panel reaktivních protilátek k lidským HLA antigenům, zvýšená hladina ukazuje na možné riziko rejekce štěpu), a jiné další vyšetření dle konkrétního pacienta.
Kontraindikace transplantace srdce. I když jsou udávány přesné charakteristiky, které kontraindikují pacienta k podstoupení transplantace, vždy je nutné individuální zhodnocení rozsahu a míry dané kontraindikace a vliv na další prognózu u každého pacienta. Patří sem:
- probíhající nebo chronická infekce
- jiné závažné onemocnění (malignita v posledních 5 letech, v případě vyléčeného onemocnění lze tuto dobu zkrátit)
- fixovaná plicní hypertenze (plicní cévní rezistence > 4 Woodove jednotky, transpulmonální gradient >20 mmHg)
- závislost na alkoholu
- drogová závislost
- psychóza
- BMI > 40
Relativní:
- věk nad 60-65 let
- diabetes mellitus s orgánovými komplikacemi
- povšechná ateroskleróza
- předpoklad špatné spolupráce (nedodržování léčebného režimu a životosprávy, poruchy chování, deprese)
- špatné sociální zázemí
- BMI > 30
Příjemce musí být schopný aktivní spolupráce s transplantačním týmem a v případě nálezu dárce se včas dostavit do transplantačního centra. Příjemci, kteří jsou v kritickém stavu, vyžadují hospitalizaci na jednotce intenzivní péče, často s inotropní farmakologickou podporou, v nejzávažnějších případech i zavedení mechanické oběhové podpory v režimu „Bridge to Transplant“ (viz níže). Tito pacienti jsou následně upřednostněni při nabídce dárce před stabilními pacienty na čekací listině.
DÁRCE
V legislativě České republiky, konkrétně v zákoně č. 285/2002 Sb., je ustanoveno, že jedinou podmínkou k odběru je stanovení smrti potencionálního dárce. Není nutný předchozí souhlas s dárcovstvím. Pokud však pacient před smrtí prokazatelně vyslovil nesouhlas s posmrtným odběrem tkání a orgánů, není možné k výkonu přistoupit. Pokud blízké osoby zemřelého nesouhlasí s odběrem, není to dle zákona povinné zohlednit, avšak z etického hlediska to zůstává problémem.
Za potencionálního dárce srdce je považovaný každý jedinec s prokázanou mozkovou smrtí. Je nutný však další screening k vyloučení zásadních kontraindikací znemožňujících odběr a použití srdce. Kromě vyhodnocení věku, váhy a výšky, pohlaví, ABO krevní skupiny, příčiny smrti, biochemického, hematologického a imunologického vyšetření krve se provádí i RTG hrudníku, EKG, echokardiografie, ev. katetrizační vyšetření pravostranných srdečních oddílů nebo koronárních cév (u starších pacientů). Ke kontraindikacím řadíme:
- věk >50-60 let (relativní kontraindikace)
- prolongovaná srdeční zástava, hypotenze, závažné trauma hrudníku s důkazem poškození srdce, intrakardiální injekce
- preexistující onemocnění srdce
- extracerebrální malignita nebo glioblastom
- pozitivita serologie na HIV, HBV; pozitivita HCV u dárce dnes již není kontraindikace
- abúzus alkoholu a drog - nutné individuální zhodnocení
Mozková smrt je provázená „autonomní a cytokinovou bouří“, která vede k hemodynamické nestabilitě na podkladě autonomní dysfunkce, relativní hypovolemie při vazodilataci, hypotermie a dysrytmií. Je nutná agresivní volumoterapie, podávání inotropik a vazoaktivních látek, doporučuje se i hormonální resuscitace (methylprednison + trijodthyronin + vazopresin). Samozřejmostí je umělá plicní ventilace, ohřívání těla dárce, širokospektrální antibiotická terapie.
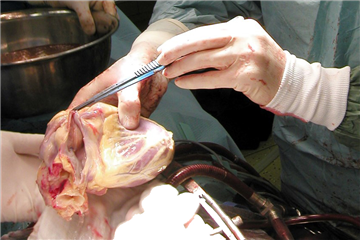
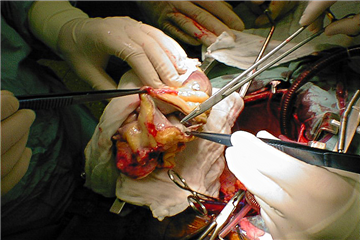
Odběr srdce k transplantaci. Definitivní zhodnocení dárce a transplantátu provádí odběrový tým. Po otevření hrudníku, vypreparování a mobilizaci srdečních struktur následuje inspekční a palpační zhodnocení stavu srdce. Navodí se plná antikoagulace systémovým podáním nefrakcionovaného heparinu (jako u standardní srdeční operace) a přistupuje se k samotnému odběru srdce. Nejprve se podává kardioplegický roztok, během čeho se nastřihne dolní dutá žíla a ouško levé síně, aby nedošlo k dilataci srdečních oddílů. Po ukončení jeho podávání se kompletně oddělí dolní dutá žíla. Po nadzvednutí srdce kraniálně se protnou plicní žíly vstupující do levé síně. Oddělí se plicnice, aorta a jako poslední se odděluje horní dutá žíla. Štěp je ještě jednou zkontrolován pro eventuální patologie (chlopenní vady, foramen ovale patens). Srdce je vloženo do konzervačního roztoku o nízké teplotě (4-10°C) a transportováno do centra, k provedení samotné transplantace. Tolerována doba ischemie je 4-6 hodin.

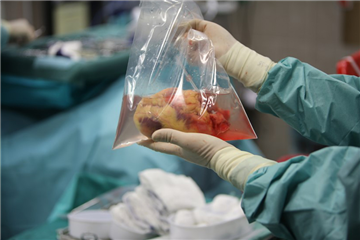
Kompatibilita dárce a příjemce. Základním kritériem je shoda v ABO krevní skupině (v případě inkompatibility hrozí hyperakutní rejekce štěpu). Hmotnost dárce by se měla od hmotnosti příjemce lišit ideálně do 20%. Vzhledem k různé hmotnosti srdce u mužů a žen se dnes spíše řídime pomocí „predicted heart mass“ indexu (https://transplanttoolbox.shinyapps.io/calcphm/). Provádění jiných testů, zejména vyšetření kompatibility HLA antigenů, je z důvodu omezených časových možností prováděno jen v některých centrech.
Technika srdeční transplantace
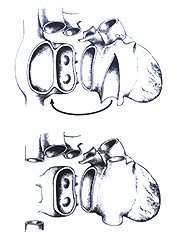 Specifickým rysem srdeční transplantace je organizačně náročná koordinace odběru a transportu dárcovského srdce a současně výběr a příprava optimálního příjemce k operaci tak, aby se zbytečně neztrácel ischemický čas štěpu. Samotná technika operace má dvě základní varianty. Klasická technika ortotopické srdeční transplantace dle Shumwaye (biatriální technika) byla zlatým standardem až do poloviny 90. let, v některých centrech se provádí do dnešní doby. Postupně však tento způsob nahradila bikavální technika, která je v současnosti celosvětově nejrozšířenější. Důvodem je nižší riziko poškození sinusového uzlu, lepší hemodynamické parametry a nižší riziko rozvoje trikuspidální insuficience.
Specifickým rysem srdeční transplantace je organizačně náročná koordinace odběru a transportu dárcovského srdce a současně výběr a příprava optimálního příjemce k operaci tak, aby se zbytečně neztrácel ischemický čas štěpu. Samotná technika operace má dvě základní varianty. Klasická technika ortotopické srdeční transplantace dle Shumwaye (biatriální technika) byla zlatým standardem až do poloviny 90. let, v některých centrech se provádí do dnešní doby. Postupně však tento způsob nahradila bikavální technika, která je v současnosti celosvětově nejrozšířenější. Důvodem je nižší riziko poškození sinusového uzlu, lepší hemodynamické parametry a nižší riziko rozvoje trikuspidální insuficience.
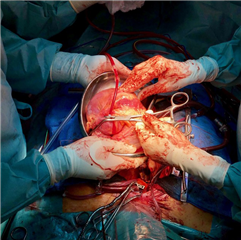
Po otevření hrudníku a zavedení kanyl mimotělního oběhu (vysoká kanylace ascendentní aorty, kanylace obou dutých žil separátně) se pacient schladí do mírné hypotermie a klampuje se ascendentní aorta. Aorta se protíná těsně nad sinotubulární junkcí, podobně i plicnice. Další postup se liší dle zvolené techniky.
Při biatriální technice se pravá i levá síň transsekují těsně nad atrioventrikulární junkcí, ponechává se tkáň obou síní příjemce. Levá síň srdce dárce se našívá k levé síni příjemce dlouhým pokračujícím stehem. Podobně se pokračuje u pravé síně, dál se našívá plicnice a jako poslední aorta.
Bikavální technika je rozdílná zejména v kompletním odstranění pravé síně příjemce. Ostrůvek levé síně s vústěním plicních žil se ponechává stejně jako při biatriální technice. Anastomózy se šijí v pořadí: levá síň, dolní dutá žíla, horní dutá žíla, plicnice, a jako poslední aorta.
Podobně u obou technik následuje důkladné odvzdušnění srdečních dutin, odstraní se klampáž aorty a srdce začíná po prokrvení koronárních cév krví znovu pracovat. V případě komorových dysrytmií se podává elektrický výboj, často je nutná extenzivní inotropní podpora. Mimotělní oběh je ukončen a sternotomie se uzavírá.

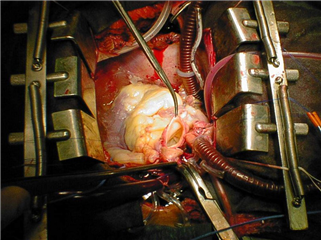

Pooperační menežment po transplantaci srdce
Allograft pooperačně často vyžaduje prolongovanou inotropní farmakoterapii ve vysokých dávkach. Je nutné si taky uvědomit, že dárcovské srdce je denervované, nereaguje proto adekvátně na autonomní regulaci při stresu, šoku nebo zátěži, je plně závislé od změny krevních hladin katecholaminů. Pooperačně se mohou vyskytovat různé arytmie - sinusová a junkční bradykardie, fibrilace síní, komorové extrasystoly. Případnou systémovou i plicní hypertenzi je nutné agresivně léčit, aby nedošlo k zbytečnému zvýšení afterloadu a zátěži štěpu. Po hemodynamické stabilizaci pacient opouští jednotku intenzivní péče, v stanoveném režimu podstupuje opakované endomyokardiální biopsie a je propuštěn do domácí péče po 3-4 týdnech. Nadále pokračuje komunikace a časté kontroly v transplantačním centru dle stanoveného schématu nebo při výskytu komplikací.
Rejekce štěpu je přirozenou reakcí imunitního systému příjemce na cizí (dárcovský) antigen. Většina reakcí je způsobená celulární imunitní odpovědí. V menší míře, ale o to závažnější, je poškození štěpu v případě humorální formy reakce. Hyperakutní rejekce nastupuje v prvních hodinách po transplantaci, vzniká nejčastěji na podkladě ABO inkompatibility, je vzácná. Ostatní formy akutní rejekce se manifestují většinou v průběhu prvních 6 měsíců po operaci, jejich časné odhalení je možné jenom pomocí endomyokardiální biopsie. Proto každý pacient po operaci musí ve stanoveném schématu toto vyšetření opakovaně podstoupit, s cílem časného zahájení antirejekční terapie. Jako profylaxe rejekce je podávána trojkombinace léčiv - takrolimus, mykofenolát mofetil a prednison. V případě výskytu rejekce štěpu jsou zahájeny další terapeutické postupy:
- pulzní terapie kortikoidy
- intravenozní antitymocytární globulin
- plazmaferéza
- podpůrný menežment dle stavu (hemodynamický monitoring, inotropní podpora...)
Infekce je hlavní příčinou morbidity a mortality v pooperačním období, zejména v prvních 3 měsících nebo po epizodách intenzivní antirejekční imunosupresivní terapie. Nejčastější jsou pneumonie, mediastinitidy a infekce operační rány, močové, kožní a katetrové infekce. Kromě běžných patogenů (Escherichia coli, Pseudomonas aeruginosa, kmeny Staphylococcus) je dominantním původcem Cytomegalovirus, nasledovaný dalšími viry (EBV, HSV), vyskytují se i houby (různé kmeny Candida a Aspergillus), protozoa (Pneumocystis carinii, Toxoplasma gondii).
Koronární nemoc štěpu. Pozdní potransplantační komplikace, rapidně se rozvíjející specifická forma aterosklerózy koronárních tepen štěpu. Od standardní koronární aterosklerózy se liší koncentrickou formou postižení, difúzním charakterem lézí, kalcifikace se vyskytují ojediněle. Vzniká pravděpodobně na podkladě kombinace imunologické reakce (rejekce štěpu) a vedlejších účinků imunosupresiv. Diagnostika je náročná z důvodu denervace srdce a tedy nepřítomnosti anginozních obtíží, ideální modalitou je pravidelné koronarografické vyšetření s využítím IVUS. Terapeuticky připadají v úvahu statiny v kombinaci s navýšením imunosupresivní terapie. Definitivní terapii je retransplantace.
Malignity patří k nejzávažnějším pozdním komplikacím transplantace srdce, resp. dlouhodobé imunosupresivní terapie. Riziko vzniku malignity je 10-100x vyšší než u zdravé populace. Nejčastěji se vyskytují lymfoproliferativní onemocnění a nádory kůže. Terapeutické možnosti zahrnují snížení dávky imunosupresiva spolu s konvenčním terapeutickým postupem (chemoterapie, radioterapie, chirurgická resekce). Postupy jsou spojeny s vysokým rizikem a limitovanou úspěšností.
VÝSLEDKY
Navzdory uvedeným komplikacím je dle dostupných dat transplantace srdce prokazatelně nejlepší léčebnou metodou terminálního srdečního selhání v porovnání s maximální konzervativní terapií a mechanickou srdeční podporou. Časná pooperační mortalita (do 30 dnů) se pohybuje mezi 5-10%, přežívání po 1 roku je 86%.
Krátkodobá podpora oběhu
Mechanická podpora cirkulace zahrnuje všechny systémy, jejichž úlohou je v různých klinických situacích zlepšení perfuze organizmu, odlehčení práce srdce a ev. zlepšení koronární perfuze. Na tomto místě je vhodné rozdělení na krátkodobé a dlouhodobé formy cirkulační podpory, jednak z důvodu rozdílných indikací, způsobu a náročnosti zavedení, a především z důvodu dlouhodobé trvanlivosti a funkčnosti.
Krátkodobá podpora oběhu je určena k rychlému obnovení orgánové perfuze. Zavedení je relativní rychlé, často perkutánní, u některých systémů je nutná chirurgická preparace cévy, nebo sternotomie a centrální zavedení. Nachází proto využití zejména v akutních, život ohrožujících situacích. Indikace k zavedení jsou nasledovné:
- profylakticky (u některých vysoce rizikových intervenčních výkonů - PCI, TAVI)
- kardiogenní šok (při infarktu myokardu a jeho mechanických komplikacích, při myokarditidě a postpartální kardiomyopatii)
- akutní dekompenzace srdečního selhání
- srdeční zástava a farmakorezistentní ventrikulární dysrytmie
- post-kardiotomicky - nemožnost ukončení mimotělního oběhu
Mechanická podpora oběhu sama o sobě není terapie příčiny hemodynamické instability. Je jí možno chápat jako přemostění doby, kterou srdce potřebuje k zotavení, nebo se blíže ozřejmí patologický stav. Strategie, v jakých je krátkodobá podpora oběhu zavedená, jsou tedy různé a označují se následovně:
- Bridge to Decision, přemostění k rozhodnutí. Nejpozději 2-3 dny po zavedení podpory je nutná její re-evaluace a rozhodnutí o další strategii (Bridge to Recovery/Bridge/Transplant, nebo rozhodnutí o ukončení terapie při infaustní prognóze). Proto se používají další pojmy:
- Bridge to Recovery, přemostění k obnovení srdeční funkce, bez nutností další mechanické oběhové podpory
- Bridge to Bridge, přemostění k implantaci dlouhodobé mechanické oběhové podpory
- Bridge to Transplant, vzácně je možná časná transplantace srdce v návaznosti na krátkodobou srdeční podporu
I když tyto metody jsou schopny poskytnout výrazné zlepšení hemodynamického stavu pacienta, jejich jednoznačný benefit stran přežívání pacientů se ukázal jenom u post-kardiotomického oběhového selhání. U ostatních indikací jsou výsledky nepřesvědčivé, přežívání neuspokojivé a doporučení nejsou ustálena. Dále budou rozebírány jednotlivé technologické varianty krátkodobé oběhové podpory.
INTRAAORTÁLNÍ BALÓNKOVÁ KONTRAPULZACE
 Perkutánně cestou a. femoralis je do descendentní aorty zavedený balón, který se na základě synchronizace s R kmitem kontinuálního EKG monitoringu insufluje v diastole a desufluje v systole. Nafouknutím v diastole se zlepšuje diastolické prokrvení koronárního řečistě a hlavových cév (tzv. diastolická augmentace). V systole aktivní desuflace způsobí snížení afterloadu, čím se sníží nároky na práci myokardu, sníží se jeho spotřeba kyslíku a napětí stěny. Antikoagulace heparinem je samozřejmou součástí managementu.
Perkutánně cestou a. femoralis je do descendentní aorty zavedený balón, který se na základě synchronizace s R kmitem kontinuálního EKG monitoringu insufluje v diastole a desufluje v systole. Nafouknutím v diastole se zlepšuje diastolické prokrvení koronárního řečistě a hlavových cév (tzv. diastolická augmentace). V systole aktivní desuflace způsobí snížení afterloadu, čím se sníží nároky na práci myokardu, sníží se jeho spotřeba kyslíku a napětí stěny. Antikoagulace heparinem je samozřejmou součástí managementu.
Kontrapulzace se nejčastěji využívá při nekontrolovatelné myokardiální ischemii, při kardiogenním šoku a při postkardiotomicky sníženém srdečním výdeji. Kontraindikací je závažná aortální regurgitace, disekce aorty, rizikové je zavedení přístroje u aorty s rozsáhlými kalcifikacemi. Komplikace jsou ischémie končetiny, přes kterou je podpora zavedena, infekce, lokální komplikace v místě vpichu (krvácení, pseudoaneuryzma, fistuly atd.)
EXTRACORPOREAL LIFE SUPPORT (ECLS)
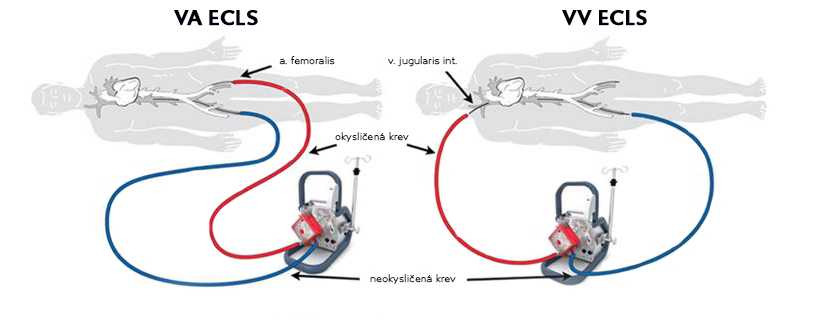
Extrakorporální životní podpora, nebo starší název extrakorporální membránová oxygenace (ECMO) je již na rozdíl od kontrapulzace pravou podporou oběhu, která zprostředkovává podporu krevního proudění k cílovým orgánům. ECLS je možné si představit jako variantu přístroje pro mimotělní oběh, který je dizajnovaný k dlouhodobějšímu použití (řádově dnů až týdnů). Z důvodu nepřítomnosti krevní stázy (chybí krevní rezervoár) a použití kanyl krytých heparinem není nutná až tak silná antikoagulace jako při standardním peroperačním použití mimotělního oběhu. Součástí přistroje jsou:
- přívodná kanyla
- oxygenátor s vestavěným výměníkem tepla
- centrifugální pumpa
- odvodní kanyla
Standardní veno-arteriální ECLS se zavádí cestou tříselných cév (a. femoralis a v. femoralis) perkutánní nebo chirurgickou cestou. Je možné i centrální zavedení do pravé síně a ascendentní aorty (při závažném aterosklerotickém periferním postižení nebo při postkardiotomickém selhání oběhu), další variantou je a.axillaris.
K zabezpečení bezpečné periferní perfuze na dané končetině se doporučuje využít boční linku pro periferní prokrvení. Z komplikací je nejčastější krvácení, které souvisí s nutností protrahované antikoagulace. Z dalších komplikací se objevuje akutní respirační a renální insuficience, bakteriémie, mediastinitida, cévní mozková příhoda, selhání oxygenátoru a nutnost výměny pumpy.
Kromě standardního veno-arteriálního zapojení existuje ještě veno-venózní varianta (v.jugularis interna a v.femoralis), která neslouží k podpoře oběhu ale jenom k podpoře oxygenace u respiračního selhání, v tomto případě tedy možno hovořit správně o ECMO, tj. extrakorporální membránové oxygenaci.
TandemHeart
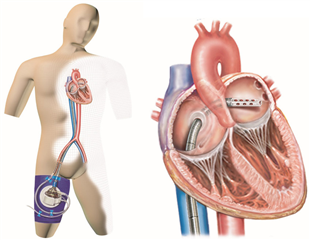 Perkutánně do tříselných cév zavedená podpora, její odvodná „žilní“ kanyla je zavedená z v. femoralis přes pravou síň transseptálně do levé síně, z které odvádí krev a tím odlehčuje práci levé komoře. Samotná centrifugální pumpa je umístěná parakorporálně. Přívodná kanyla je zavedená přes a. femoralis. Oproti ECLS tento systém poskytuje uspokojivější odlehčení levé komory. S oblibou se využívá u rizikových koronárních intervencí nebo u poinfarktového kardiogenního šoku.
Perkutánně do tříselných cév zavedená podpora, její odvodná „žilní“ kanyla je zavedená z v. femoralis přes pravou síň transseptálně do levé síně, z které odvádí krev a tím odlehčuje práci levé komoře. Samotná centrifugální pumpa je umístěná parakorporálně. Přívodná kanyla je zavedená přes a. femoralis. Oproti ECLS tento systém poskytuje uspokojivější odlehčení levé komory. S oblibou se využívá u rizikových koronárních intervencí nebo u poinfarktového kardiogenního šoku.
Impella
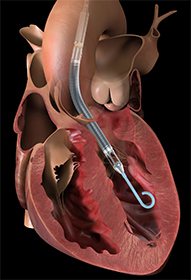 Impella je technicky odlišná varianta oběhové podpory. Jedná se o mikroaxiální pumpu, která je zavedená retrográdně přes aortální ústí z aorty do levé komory, pumpuje intraventrikulární krev přímo do aorty za aortální ústí. Poskytuje vynikající vyprázdnění levé komory, snižuje nároky na práci srdce a zlepšuje koronární perfuzi. Používá se zejména profylakticky při kardiointervenčních výkonech, kde vykazuje výrazně lepší výsledky v porovnání s kontrapulzací. Dalším využím je kardiogenní šok na podkladě těžké dysfunkce levé komory.
Impella je technicky odlišná varianta oběhové podpory. Jedná se o mikroaxiální pumpu, která je zavedená retrográdně přes aortální ústí z aorty do levé komory, pumpuje intraventrikulární krev přímo do aorty za aortální ústí. Poskytuje vynikající vyprázdnění levé komory, snižuje nároky na práci srdce a zlepšuje koronární perfuzi. Používá se zejména profylakticky při kardiointervenčních výkonech, kde vykazuje výrazně lepší výsledky v porovnání s kontrapulzací. Dalším využím je kardiogenní šok na podkladě těžké dysfunkce levé komory.
Levitronix CentriMag
 Jedná se o centrifugální pumpu s plně magneticky levitovaným otáčením. Zavádí se centrálně, chirurgicky, sternotomií, může být designovaná jako pravostranná nebo levostranná srdeční podpora. V závislosti od toho je zapojení buď pravá síň→plicnice, nebo levá síň→aorta. Kanyly jsou následně perkutánně vyvedeny na povrch těla, kde je parakorporálně uložena samotná pumpa. Využívá se u kardiogenního šoku (např. při fulminantní myokarditidě) a postkardiotomického nízkého srdečního výdeje, s úspěchem byl tak použit v strategii Bridge to Recovery nebo Bridge to Bridge. Vzhledem k delší době funkčnosti (i nad 1 měsíc), je někdy považována za střednědobou podporu.
Jedná se o centrifugální pumpu s plně magneticky levitovaným otáčením. Zavádí se centrálně, chirurgicky, sternotomií, může být designovaná jako pravostranná nebo levostranná srdeční podpora. V závislosti od toho je zapojení buď pravá síň→plicnice, nebo levá síň→aorta. Kanyly jsou následně perkutánně vyvedeny na povrch těla, kde je parakorporálně uložena samotná pumpa. Využívá se u kardiogenního šoku (např. při fulminantní myokarditidě) a postkardiotomického nízkého srdečního výdeje, s úspěchem byl tak použit v strategii Bridge to Recovery nebo Bridge to Bridge. Vzhledem k delší době funkčnosti (i nad 1 měsíc), je někdy považována za střednědobou podporu.
Dlouhodobá podpora oběhu
Dlouhodobá oběhová podpora si, podobně jako krátkodobá podpora, dává za cíl zlepšení orgánové perfuze, odlehčení práce myokardu a ev. i navýšení koronární perfuze. Jedná se o zařízení, které jsou technicky složitější k zavedení, vyžadují náročný kardiochirurgický operační výkon, na druhé straně však poskytují dlouhodobou podporu oběhu, řádově měsíců až let. Mohou být použity jako podpora levé komory (LVAD - Left Ventricular Assist Device), pravé komory (RVAD - Right Ventricular Assist Device), nebo obou komor (BiVAD - Biventricular Assist Device). Od těchto zařízení je nutné odlišit implantaci arteficiálního srdce (TAH - Total Arteficial Heart), kde se nejedná jenom o funkční, ale i o anatomickou náhradu srdce srdcem umělým.
 Technické řešení. LVAD se standardně implantuje s odvodnou kanylou do hrotu levé komory, nasleduje samotná pumpa, která se nachází intra- nebo parakorporálně dle zvoleného přístroje, přívodná kanyla je napojená na ascendentní aortu. RVAD odvádí krev z pravé síně přes čerpadlo přímo do plicnice. BiVAD je kombinací těchto metod. Při TAH je nutné odstranění vlastního myokardu komor, přístroj se našije na zbylý myokard srdečních síní. Nejedná se tedy o podporu, ale spíš o náhradu činnosti srdečních komor přístrojem.
Technické řešení. LVAD se standardně implantuje s odvodnou kanylou do hrotu levé komory, nasleduje samotná pumpa, která se nachází intra- nebo parakorporálně dle zvoleného přístroje, přívodná kanyla je napojená na ascendentní aortu. RVAD odvádí krev z pravé síně přes čerpadlo přímo do plicnice. BiVAD je kombinací těchto metod. Při TAH je nutné odstranění vlastního myokardu komor, přístroj se našije na zbylý myokard srdečních síní. Nejedná se tedy o podporu, ale spíš o náhradu činnosti srdečních komor přístrojem.
Indikace k zavedení dlouhodobé orgánové podpory je, podobně jako u transplantace srdce, terminální srdeční selhání refrakterní ke konzervativním léčebným postupům. Pro tento účel byl vyvinut klasifikační systém klinických profilů pacientů se závažným srdečním selháním INTERMACS, který překračuje rozsah této práce. Principiálně se jedná o pacienty nereagující na adekvátní farmakoterapii, často vyžadující inotropní podporu nebo zavedení krátkodobé mechanické podpory oběhu, ejekční frakce levé komory je <25% a vrcholová spotřeba kyslíku <14 ml/kg/min.
!CAVE! Akutní kardiogenní šok nebo akutní dekompenzace srdečního selhání jsou indikací k zavedení krátkodobé mechanické oběhové podpory. Dlouhodobá podpora se implantuje, pokud možno, vždy v režimu plánované operace.
Kontraindikace k zavedení dlouhodobé podpory jsou ireverzibilní orgánová dysfunkce, závažná hemodynamická nestabilita (v tomto případě je indikováno zavedení krátkodobé podpory oběhu), koagulopatie, komplexné vrozené vady, restriktivní kardiomyopatie (zmenšené srdeční rozměry), aktivní infekce a bakteriémie (riziko infikování přístroje).
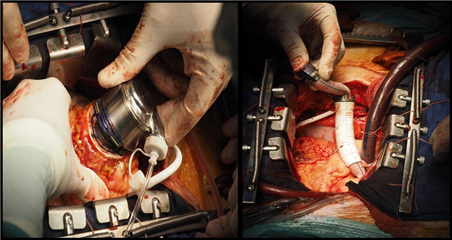
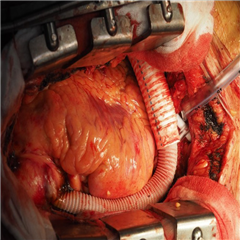

Strategie zavedení dlouhodobé oběhové podpory jsou nasledovné:
- Bridge to Transplant
- Destination Therapy
Bridge to Transplant byla jedna ze zásadních motivací vývoje dlouhodobé mechanické podpory. Cílem je přemostění doby do nalezení dárce u pacientů indikovaných k transplantaci. Bylo dokázáno, že použití mechanické podpory výrazně zlepšuje přežívání pacientů s terminálním srdečním selháním před transplantací oproti samotné medikamentózní terapii. Zároveň, posttransplantační přežívání není použitím této podpory nijak negativně ovlivněno, spíše naopak.
Destination Therapy je alternativní terapeutická modalita u pacientů s terminálním srdečním selháním, kteří jsou ale kontraindikování k srdeční transplantaci (například fixována plicní hypertenze nebo morbidní obezita). Dlouhodobá podpora oběhu je implantována doživotně. Jelikož se již prokázalo, že dlouhodobá podpora oběhu i u této skupiny pacientů výrazně zlepšuje přežívání oproti samotné lékové terapii, nabyla tato strategie v posledních letech na oblibě. Recentní studie ukazují, že dokonce již představuje častěji volenou strategii pro implantaci než Bridge to Transplant.
Fluktuace strategie. Je nutné podotknout, že i když jsou na začátku tyto strategie pevně stanoveny, je možné, že v dalším průběhu se strategie u pacienta změní. Například obézní pacient, který byl „odsouzený“ na doživotní mechanickou podporu, je přehodnocen a může podstoupit transplantaci (pokud je nad touto možností pomýšleno již od začátku, může se této strategii říkat Bridge to Candidacy). Vzácnou, ale možnou variantou je zotavení z terminálního srdečního selhání, obnova dostatečné srdeční činnosti s následnou možností odpojení oběhové podpory (jedná se tedy o Bridge to Recovery).
VOLBA PŘÍSTROJE
Technologie dlouhodobé podpory oběhu prošli velkým technickým vývojem, který je spojen s dramatickým snížením morbidity a mortality. Rozlišujeme 3 generace dlouhodobých mechanických srdečních podpor:
- generace: pumpy generující pulzatilní průtok (HeartMate I, Thoratec Paracorporeal VAD, Novacor, Berlin Heart ExCor). Za cenu zachování pulzatilního toku se vyráběly tyto relativně robustní a hlučné zařízení s nutností parakorporálního vyvedení, s větší mírou opotřebování a náchylností ke komplikacím. V současnosti se již vyrábí pouze Berlin Heart ExCor, které má využití u pediatrické populace.
- generace: axiální pumpy generující kontinuální průtok (HeartMate II, Jarvic 2000, Berlin Heart InCor). Z důvodu výrazně jednodušší konstrukce nevyžadující tolik prvků jsou tyto pumpy kompaktnější, pomaleji se opotřebují, umožňují jednodušší implantaci, bez nutnosti extrakorporálního vyvedení (kromě síťové linky). Žádný výrazně negativní dopad kontinuálního průtoku nebyl prokázán.
- generace: centrifugální magneticky levitované pumpy generující kontinuální průtok (HeartWare, HeartMate 3). Nejkompaktnější konstrukce umožňuje intraperikardiální implantaci. HeartWare vykazuje výsledky porovnatelné s 2. generací. HeartMate 3 však díky rychlým změnám rychlosti rotace napodobuje pulzatilní tok krve, má výrazně nižší dlouhodobou morbiditu oproti předchozí generaci při porovnatelné mortalitě. V současnosti se zdá být nejslibnější technickou variantou.
 Výsledky implantace dlouhodobé srdeční podpory jsou velice uspokojivé. Recentní data informují o 85% přežívání 1 roku, zejména u nejnovějších zařízení s kontinuálním prouděním. Za komplikace spojené s dlouhodobou oběhovou podporou a nutností užívání antikoagulace považujeme:
Výsledky implantace dlouhodobé srdeční podpory jsou velice uspokojivé. Recentní data informují o 85% přežívání 1 roku, zejména u nejnovějších zařízení s kontinuálním prouděním. Za komplikace spojené s dlouhodobou oběhovou podporou a nutností užívání antikoagulace považujeme:
- krvácení (časné pooperační, pozdní je nejčastěji gastrointestinální)
- trombóza pumpy (nutnost výměny pumpy nebo systémové trombolýzy)
- selhání pravé komory při zavedeném LVAD (sníží se sice afterload, ale zvýší se preload pravé komory, je nutná farmakoterapie, zavedení pravostranné podpory nebo transplantace srdce)
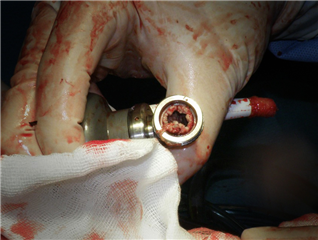
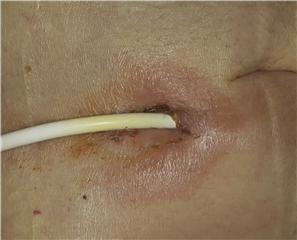
- infekce transkutánně vyvedeného síťového kabelu nebo samotné pumpy (ATB terapie až výměna pumpy)
- neurologické dysfunkce
- renální selhání
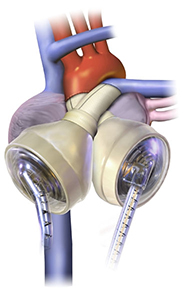 Totální arteficiální srdce (TAH) představuje další variantu, která je rezervována jenom pro některé pacienty (nejnovější doporučené postupy udávají neopravitelné vrozené srdeční vady nebo rupturu srdce). Jediným používaným přístrojem je SynCardia TAH, která představuje propojení 2 pneumaticky poháněných pulzatilních pump. Podobně jako u ostatních pulzatilních přístrojů má relativně robustní strukturu, jednou ze zásadních limitací k její implantaci je tedy dostatečný prostor v hrudníku. Využívá se jako bridge to transplant, i jako destination therapy u oboustranného srdečního selhání. V součanosti bylo TAH implantováno již téměř 2000 krát. Výsledky jsou relativně uspokojivé, 72% pacientů se dožije transplantace, medián přežití se udává na 554 dní.
Totální arteficiální srdce (TAH) představuje další variantu, která je rezervována jenom pro některé pacienty (nejnovější doporučené postupy udávají neopravitelné vrozené srdeční vady nebo rupturu srdce). Jediným používaným přístrojem je SynCardia TAH, která představuje propojení 2 pneumaticky poháněných pulzatilních pump. Podobně jako u ostatních pulzatilních přístrojů má relativně robustní strukturu, jednou ze zásadních limitací k její implantaci je tedy dostatečný prostor v hrudníku. Využívá se jako bridge to transplant, i jako destination therapy u oboustranného srdečního selhání. V součanosti bylo TAH implantováno již téměř 2000 krát. Výsledky jsou relativně uspokojivé, 72% pacientů se dožije transplantace, medián přežití se udává na 554 dní.
Další možností je nové biokompatibilní TAH CARMAT. Implantace této podpory je nyní ve fázi klinické studie (studie PIVOTAL).
Zdroje:
- Cohn LH, Adam DH. Cardiac Surgery in the Adult, Fifth Edition. New York: McGraw Hill Education, 2016. ISBN 978-0-07184487-1.
- Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JG, Coats AJ et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal 2016; 37: 2129-2200. doi:10:1093/eurheartj/ehw128.
- Schramm R, Morshuis M, Schoenbrodt M, Boergermann J, Hakim-Meibodi K, Hata M et al. Current perspectives on mechanical circulatory support. European Journal of Cardio-Thoracic Surgery 2019; 0: 1-7. doi:10.1093/ejcts/ezy444.
- Málek I. Péče o nemocné po transplantaci srdce. Intervenční a akutní kardiologie 2006; 5: 116-121.
- Ayub-Ferreira SM. Executive Summary - Guidelines for Mechanical Circulatory Support of the Brazilian Society of Cardiology. Arquivos Brasileiros de Cardiologia 2018; 111(1)4-12.
- Schäfers HJ. Klinische Grundlagen der Herz- und Throaxchirurgie, 4., aktualisierte und ergänzte Auflage. Berlin: ABW Wissenschaftsverlag GmbH, 2011. ISBN: 978-3-940615-21-3.
- Napp LC, Kühn C, Hoeper MM, Vogel-Claussen J, Haverich A, Schäfer A et al. Cannulation strategies for percutaneous extracorporeal membrane oxygenation in adults. Clinical Research in Cardiology 2016; 105: 283-296. doi:10.1007/s00392-015-0941-1.
- Birks EJ. Intermediate- and long-term mechanical circulatory support. UpToDate 2019. https://www.uptodate.com/contents/intermediate-and-long-term-mechanical-circulatory-support
- Jeevanandam V, Eisen HJ, Pinto DS. Short-term mechanical circulatory assist devices. UpToDate 2019. https://www.uptodate.com/contents/short-term-mechanical-circulatory-assist-devices
- United Network for Organ Sharing. https://unos.org/data/transplant-trends/
Za praktickou konzultaci ohledně srdeční transplantace a využití mechanických oběhových podpor děkujeme MUDr. Michalovi Smetanovi, Ph.D., lékaři Kardiochirurgické kliniky Fakultní nemocnice Hradec Králové, předtím dlouhodobě pracujícího v Instututu Klinické a Experimentální Medicíny (IKEM) v Praze.
Velké díky patří doc. MUDr. Ondřeji Szarszoiovi, Ph.D., zástupci přednosty Kardiocentra IKEM Praha za poskytnutí fotodokumentace, praktickou konzultaci a kontrolu správnosti výukových textů.
